糖化酶研究进展与趋势有何新突破?
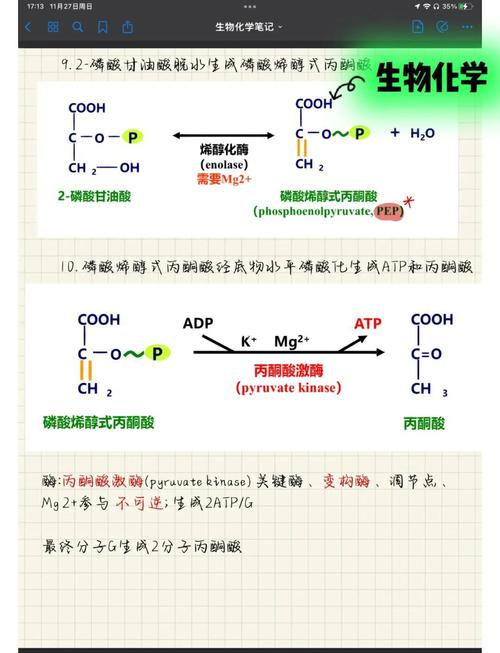
糖化酶,系统名称为α-1,4-葡萄糖苷水解酶(EC 3.2.1.3),是工业上最重要、应用最广泛的酶制剂之一,它的主要功能是随机水解淀粉、糊精等碳水化合物中的α-1,4-糖苷键,从非还原末端依次切下葡萄糖单元,最终将淀粉转化为葡萄糖,它在食品、发酵、制药、生物能源等众多领域扮演着“生物转化核心引擎”的角色。
(图片来源网络,侵删)
以下是糖化酶的研究进展及未来趋势的详细分析:
第一部分:研究进展
糖化酶的研究主要集中在菌种改良、酶学性质优化、高效表达系统构建以及应用工艺创新四个方面。
菌种选育与改良
这是糖化酶研究的源头和基础,目标在于获得高产、高活性、高稳定性及特殊底物谱的菌株。
- 传统诱变育种: 早期主要采用物理(如紫外线、γ-射线)或化学(如亚硝基胍)诱变方法,结合高通量筛选,对生产菌(如黑曲霉 Aspergillus niger、根霉 Rhizopus spp.)进行改良,该方法至今仍在使用,操作相对简单,但具有随机性和盲目性。
- 基因工程与代谢工程:
- 过表达关键基因: 通过克隆糖化酶的结构基因(glaA等)及其强启动子(如 glaA 自身启动子、 pgkA 启动子),构建表达载体导入宿主,实现糖化酶的过量表达,这是目前提高产量的主流技术。
- 敲除竞争途径基因: 通过敲除或抑制与糖化酶生产竞争碳源或能量的代谢途径基因(如淀粉合成途径、柠檬酸循环关键酶基因),将更多的代谢流导向糖化酶的合成。
- 转录因子调控: 挖掘和改造参与糖化酶合成的关键转录因子(如 XlnR、 CreA),通过过表达激活型转录因子或敲除抑制型转录因子,从全局调控层面大幅提升产量。
- 蛋白质工程:
- 理性设计: 基于糖化酶的晶体结构和催化机理,通过定点突变、饱和突变等方法,定向改造其关键氨基酸残基,以提升其热稳定性、酸碱耐受性、底物亲和力(Km值)、催化效率(kcat/Km值)等。
- 定向进化: 在体外模拟自然进化过程,通过对基因进行随机突变(如易错PCR、DNA shuffling)和构建突变文库,结合高通量筛选技术,筛选出性能更优的突变体,该方法不依赖于结构信息,适用性广。
高效表达系统构建
为了满足工业化大规模生产的需求,构建高效、稳定、低成本的表达系统至关重要。
(图片来源网络,侵删)
- 真菌表达系统: 以黑曲霉和毕赤酵母(Pichia pastoris)为代表。
- 黑曲霉: 作为传统宿主,其自身分泌系统强大,且分泌的糖化酶能正确进行翻译后修饰(如糖基化),得到的酶性质天然,但菌种遗传背景相对复杂,基因操作难度稍大。
- 毕赤酵母: 近年来异源表达糖化酶的明星宿主,其优点是遗传操作简单、生长速度快、高密度发酵能力强、能进行甲醇诱导的高水平表达,通过优化信号肽(如α-因子信号肽)、基因拷贝数和发酵条件,毕赤酵母表达的糖化酶产量可达数克/升,极具工业应用价值。
- 细菌表达系统: 如大肠杆菌(E. coli),虽然其遗传操作极为成熟,但糖化酶作为真核蛋白,在大肠杆菌中易形成包涵体,需要复杂的复性过程才能恢复活性,且其糖基化修饰与天然酶不同,可能导致酶学性质差异,通常用于酶的结构和功能研究,而非大规模生产。
酶学性质与应用工艺优化
- 酶学性质改造:
- 热稳定性: 通过蛋白质工程,提高糖化酶在高温下的稳定性,使其在液化淀粉的高温工艺(>90°C)中保持活性,减少冷却步骤,简化工艺,降低能耗。
- 酸碱耐受性: 改造糖化酶,使其在更宽的pH范围内(尤其是酸性条件下)保持高活性,以适应不同发酵体系(如酒精发酵的酸性环境)。
- 底物特异性: 改造糖化酶,使其对支链淀粉的α-1,6-糖苷键(分支点)有更好的“切支”能力,或能直接作用于液化程度较低的淀粉,从而减少普鲁兰酶的使用,降低生产成本。
- 应用工艺创新:
- 糖化工艺的连续化与智能化: 开发固定化糖化酶技术,将酶固定在载体上,构建填充床或流化床反应器,实现连续生产,提高酶的稳定性和利用率,便于自动化控制。
- “液化-糖化”同步进行(SSF): 在酒精发酵等工艺中,利用耐高温的糖化酶和耐高温的酿酒酵母,将液化、糖化和发酵三个步骤在同一个反应器中同时进行,这可以显著缩短生产周期,减少染菌风险,提高酒精产率。
第二部分:未来趋势
随着生物技术和相关学科的飞速发展,糖化酶的研究和应用正朝着更高效、更智能、更绿色的方向迈进。
高性能酶的定向创制
- AI驱动的蛋白质设计: 传统的蛋白质工程依赖试错,效率低下。人工智能(AI)和机器学习(ML)将被广泛应用于糖化酶的设计,通过深度学习模型预测蛋白质结构与功能关系,可以精准预测有益突变位点,甚至从头设计全新的、具有特定功能的糖化酶,实现从“经验试错”到“理性设计”的飞跃。
- 多酶复合体/人工细胞工厂的设计: 未来的趋势不再是单一酶的优化,而是构建“多酶级联反应系统”,将α-淀粉酶、糖化酶、普鲁兰酶甚至纤维素酶等基因融合表达,或将不同酶在纳米载体上进行有序组装,模拟细胞内的代谢通道,实现淀粉到葡萄糖的高效、协同转化,减少中间产物的抑制,极大提升转化效率。
绿色生物制造过程的整合
- 非粮生物质的高值化利用: 随着粮食安全问题的凸显,利用秸秆、木薯、玉米芯等农业废弃物作为原料生产燃料乙醇和化学品成为必然趋势,未来的糖化酶研究将更加关注其在纤维素和半纤维素降解中的作用,或者开发能同时降解多种生物质组分的“多功能糖化酶”。
- “酶法+AI”的智能发酵: 将先进的酶制剂与物联网(IoT)、大数据分析相结合,构建智能发酵工厂,通过实时监测发酵过程中的底物浓度、酶活、产物生成等数据,利用AI算法动态调控补料、溶氧、温度等参数,实现糖化酶生产及其应用过程的全局最优控制,达到降本增效、节能减排的目的。
应用领域的拓展与深化
- 高附加值产品合成: 糖化酶不仅是生产葡萄糖的工具,更是构建更复杂分子的“砌块”,利用糖化酶或其改造体催化合成功能性低聚糖(如低聚异麦芽糖、低聚龙胆糖)、稀有糖(如阿洛酮糖)以及糖基化修饰的药物中间体等,是未来的重要发展方向。
- 生物炼制中的核心地位: 在未来的生物炼制产业中,糖化酶将作为核心催化剂,将廉价的生物质平台转化为生物基材料(如聚乳酸PLA)、生物基化学品(如乳酸、丁二酸)和生物基能源,推动化工行业从“石油基”向“生物基”的战略转型。
新型表达系统的探索
- 细胞工厂的再优化: 除了毕赤酵母,丝状真菌(如里氏木霉 Trichoderma reesei)作为高效的分泌表达系统,其潜力将进一步被挖掘,通过对其分泌途径进行深度改造,有望实现更高水平的蛋白分泌。
- 无细胞合成生物学: 无细胞系统避免了细胞生长和维持的能量消耗,理论上可以实现更高的产物浓度和转化效率,开发基于无细胞体系的糖化酶合成与催化系统,将为极端条件下的生物催化和快速定制化酶生产提供新思路。
糖化酶的研究已经从传统的菌种改良和发酵优化,进入了以基因工程、蛋白质工程和合成生物学为核心的精准设计时代,未来的研究将更加注重多学科交叉融合,特别是AI技术的深度介入,推动糖化酶向更高性能、更广谱适用、更智能集成的方向发展,其应用也将从传统的淀粉水解,拓展到更广阔的生物质精炼和绿色化学品合成领域,在全球可持续发展中扮演越来越重要的角色。
(图片来源网络,侵删)
文章版权及转载声明
作者:99ANYc3cd6本文地址:https://bj-citytv.com/post/2228.html发布于 2025-12-24
文章转载或复制请以超链接形式并注明出处北京城市TV