投资干细胞行业政策风险
下面我将从政策风险的核心来源、具体表现、投资应对策略三个方面,为您进行详细剖析。
(图片来源网络,侵删)
政策风险的核心来源
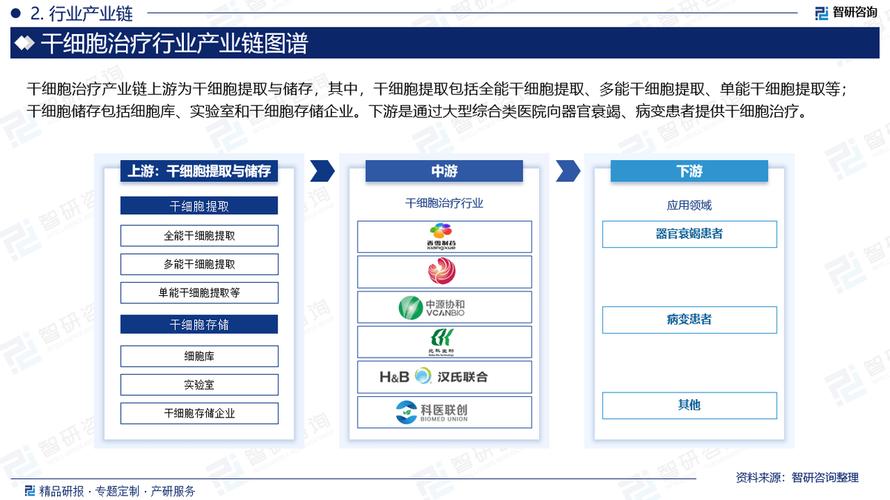
干细胞行业的政策风险主要源于其技术的前沿性、伦理的敏感性以及医疗应用的特殊性,这决定了政府必须采取非常审慎和严格的监管态度。
-
技术前沿性与未知性
- 风险点:干细胞技术发展日新月异,其长期安全性、有效性、潜在的致瘤性等科学问题尚未完全明确,政府对一项不完全了解的、可能颠覆现有医疗体系的技术,天然会持保守和观望态度。
- 政策体现:倾向于将干细胞治疗归类为“临床研究”而非“常规医疗”,禁止商业化应用,直到有足够的高级别临床证据。
-
伦理与道德争议
- 风险点:尤其是胚胎干细胞的研究,涉及到人类胚胎的来源和使用,触及了社会伦理和宗教信仰的敏感神经,这引发了巨大的社会争议和公众担忧。
- 政策体现:各国政府对胚胎干细胞的研究设立了严格的限制,如禁止生殖性克隆、规定胚胎干细胞的来源和使用的伦理审查程序等,这种伦理红线一旦触碰,可能导致项目被叫停,甚至立法禁止。
-
医疗安全与患者权益
(图片来源网络,侵删)- 风险点:干细胞治疗的“神奇疗效”吸引了大量饱受疾病折磨的患者,但也催生了大量的“游医”和“黑诊所”,这些机构夸大宣传、违规操作,不仅给患者带来了健康和经济上的巨大损失,也严重扰乱了市场秩序,并引发了严重的社会负面事件。
- 政策体现:政府为了保护公众健康,会采取“一刀切”或严格限制的监管政策,叫停所有未经批准的临床试验,对违规机构进行严厉打击,这会直接影响到合法企业的生存环境。
-
监管体系的滞后性与复杂性
- 风险点:干细胞技术是交叉学科,涉及医学、生物学、药学等多个领域,传统的药品(如化药、生物药)和医疗器械监管体系可能不完全适用,建立一个既能鼓励创新又能确保安全的、全新的监管框架,需要漫长的探索和试错过程。
- 政策体现:法规政策多变、审批流程不透明、标准不统一,企业可能投入巨资研发,但等到政策明朗时,市场机会可能已经消失。
政策风险的具体表现
政策风险最终会通过以下几种方式,直接转化为企业的经营风险和投资人的财务风险。
-
准入与审批风险
- 临床研究审批:开展干细胞临床研究需要经过国家卫健委和国家药监局(NMPA)的联合审批,这个过程极其严格,耗时漫长(数年甚至更久),且通过率极低,许多企业研发的产品可能永远无法进入临床阶段。
- 药品/医疗器械注册:如果干细胞产品被定义为“药品”(如CAR-T细胞疗法),则需要按照NMPA的药品注册路径进行申报,除了少数造血干细胞产品外,绝大多数干细胞治疗产品尚未获批上市,这意味着企业无法进行合法的商业化销售,无法产生收入。
-
商业化禁令风险
(图片来源网络,侵删)- “禁止令”与“限制令”:这是干细胞行业最典型的政策风险,在很长一段时间里,中国政府对干细胞临床研究和应用采取了“暂停”和“严格限制”的态度,国家卫健委曾发文要求所有医疗机构和科研机构停止未经批准的干细胞临床研究,对于依赖于此业务的企业,这无异于“釜底抽薪”。
- 支付体系缺失:即使有产品获批,如果不能被纳入国家医保或商业保险的报销目录,患者将需要自费承担高昂的治疗费用(通常在10万-30万人民币),这将严重限制市场的接受度和产品的渗透率。
-
政策方向突变风险
- “开闸”与“收紧”:干细胞行业的政策环境并非一成不变,政府可能会根据技术进展、社会反馈和国际形势,在“鼓励创新”和“加强监管”之间摇摆,在某些时期,政策可能释放出鼓励的信号,资本大量涌入;但一旦出现负面事件,政策可能迅速收紧,导致行业“急刹车”,企业估值暴跌。
- 地方与中央政策冲突:一些地方政府为了吸引投资,可能会出台一些地方性的扶持政策,甚至默许一些未经批准的临床应用,但一旦中央监管部门加强执法,这些地方性的“灰色地带”业务将面临被取缔的风险。
-
知识产权与标准缺失风险
- 专利保护不力:干细胞技术的核心在于其分离、培养、扩增和诱导分化的技术方法,如果缺乏清晰、强有力的专利保护,企业的核心技术和商业模式很容易被模仿和复制,失去竞争优势。
- 行业标准缺失:缺乏统一的干细胞产品质量控制标准、制备工艺规范和疗效评价体系,导致市场鱼龙混杂,劣币驱逐良币,这既不利于行业健康发展,也增加了监管的难度。
投资应对策略
面对如此复杂和多变的政策风险,投资者需要采取更加审慎和专业的策略。
-
深入研究,紧跟动态
- 核心任务:必须将政策研究作为投资决策的首要环节,密切关注国家卫健委、科技部、国家药监局等官方部门的政策文件、新闻发布会和专家解读。
- 信息渠道:订阅行业权威媒体(如医药魔方、动脉网等)、参加行业高端峰会、与监管部门的智库或专家保持沟通。
-
选择“政策友好型”赛道
- 技术路径:优先投资于技术路径相对清晰、伦理争议较小的领域。
- 间充质干细胞:来源广泛(如脐带、胎盘、脂肪),伦理问题小,是目前临床研究和应用最多的方向。
- 非胚胎干细胞:如诱导多能干细胞,避开了胚胎的伦理问题,是未来的重要发展方向。
- 体外诊断:投资于干细胞相关的检测试剂、质控品等,这类产品监管相对宽松,且是干细胞治疗普及的必要配套。
- 应用领域:优先布局政策鼓励或监管相对宽松的领域,如美容、护肤、关节修复等“轻医疗”应用,而非直接挑战“重大疾病治疗”红线。
- 技术路径:优先投资于技术路径相对清晰、伦理争议较小的领域。
-
评估企业的“政策应对能力”
- 合规意识:考察企业管理层是否具备极强的法律和合规意识,是否将合规经营放在首位,坚决规避那些试图通过“关系”或“擦边球”运作的企业。
- 政府关系:虽然“找关系”不可取,但企业是否有能力与监管机构进行专业、透明的沟通,积极参与政策制定的讨论,是一个重要的加分项。
- 临床资源:企业是否拥有与顶尖医院(如301医院、协和医院等)合作的资源,因为这些医院往往是政策试点和临床试验的首选,能第一时间获取政策风向。
-
采用“分阶段、里程碑式”的投资
- 避免All-in:不要对处于早期研发阶段的企业进行重仓投入,因为政策风险在早期最高,任何一次政策变动都可能让项目前功尽弃。
- 设定里程碑:投资应与企业发展的关键里程碑挂钩,只有当企业成功获得国家药监局的临床试验批件,或者完成了I期临床且安全性数据良好后,下一轮投资才能解锁,这能有效控制风险敞口。
-
关注“出海”机会
- 分散风险:国内政策风险高,可以关注那些积极布局海外市场的企业,中东(如阿联酋、沙特)、东南亚、日本等国家和地区对干细胞技术的接受度更高,政策环境相对灵活。
- 获取海外认证:如果企业的产品能获得美国FDA、欧盟EMA等发达市场的认证,不仅能证明其安全性和有效性,也能为其未来在国内的政策松动时抢占先机奠定基础。
投资干细胞行业,本质上是在投资政策的风向,这是一个高风险、高潜在回报,但政策天花板效应极其明显的领域,投资者必须放弃“技术至上”的传统思维,将“政策解读能力”放在与“技术判断能力”同等重要的位置。
在当前及未来很长一段时间内,“合规是生命线,创新是主旋律,出海是避风港”,将是投资干细胞行业规避政策风险的核心逻辑。
文章版权及转载声明
作者:99ANYc3cd6本文地址:https://bj-citytv.com/post/2483.html发布于 2025-12-27
文章转载或复制请以超链接形式并注明出处北京城市TV