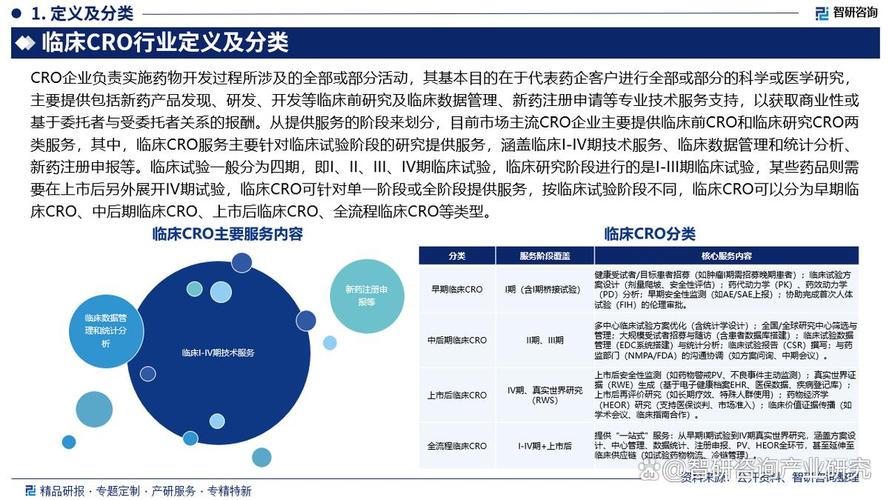
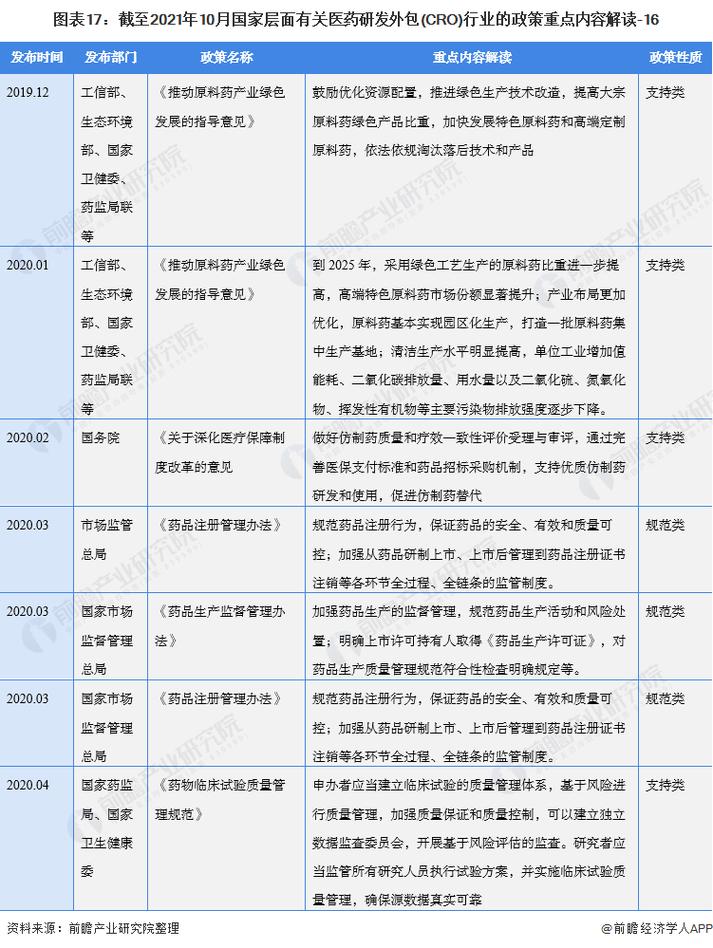
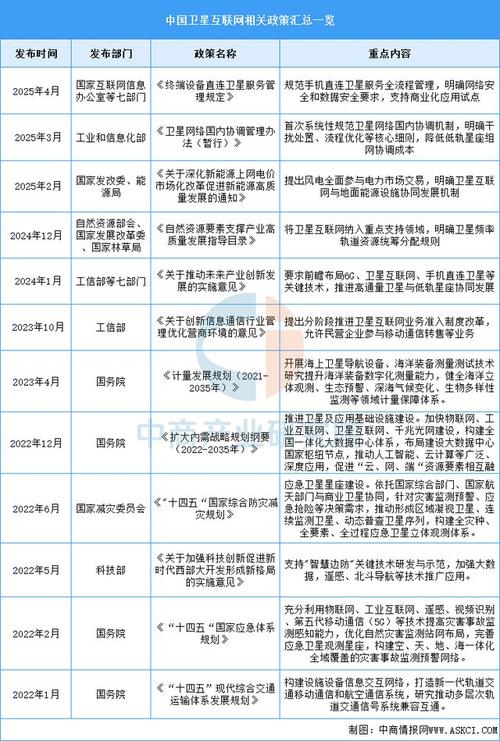
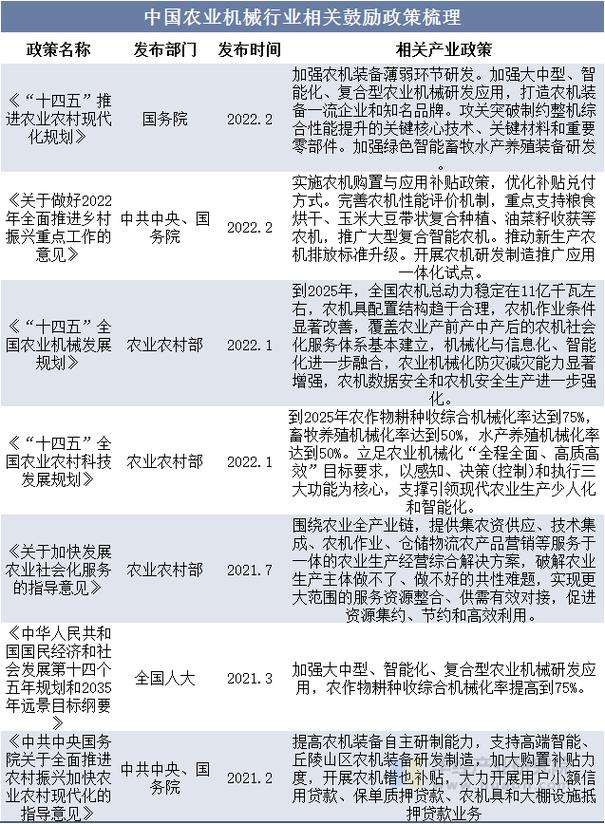
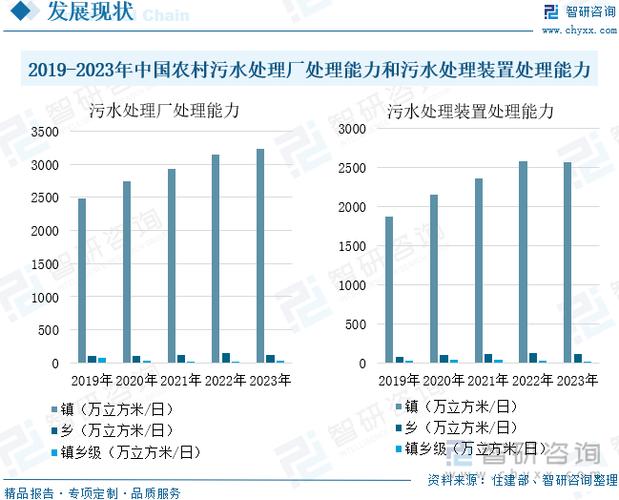
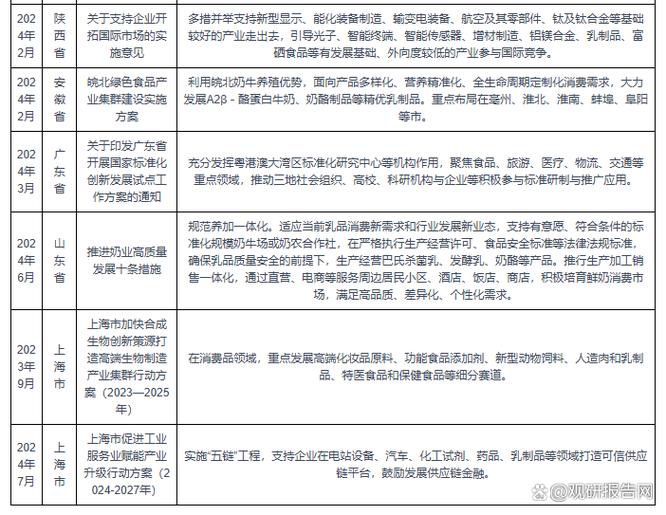
哪些政策直接影响CRO企业发展?
以下是直接影响CRO企业发展的几大类核心政策,我将从“驱动力”和“约束力”两个维度进行阐述。
(图片来源网络,侵删)
核心驱动力政策 (利好CRO发展)
这类政策旨在鼓励创新、提升研发效率,从而直接催生和扩大了对CRO服务的需求。
药品/医疗器械审评审批制度改革
这是对CRO行业最直接、最核心的驱动力。
- 具体政策:
- 优先审评审批制度: 对具有明显临床价值的创新药、临床急需药品等开设“绿色通道”,大幅缩短上市时间。
- 加速审批/附条件批准: 允许在确证性临床阶段有条件地批准上市,加速了新药上市进程。
- MAH(药品上市许可持有人)制度: 这是里程碑式的政策,它允许研发机构(而非必须由生产企业)持有药品批文,催生了大量“轻资产”的创新型Biotech公司,这些公司自身没有完整的研发和生产能力,从临床前研究、临床试验到上市后监测,都高度依赖外部CRO服务,为CRO行业带来了海量的“订单”。
- 对CRO的影响:
- 需求激增: 创新药和临床急需药品的审评加速,意味着企业需要更快地完成临床试验,CRO的服务需求量暴增。
- 业务范围扩大: MAH制度释放了研发主体的活力,使得CRO的服务链条从单纯的临床试验(CRO)扩展到覆盖从早期研发到商业化生产的全生命周期服务(CDMO/CMO)。
国家创新驱动与产业扶持政策
这类政策从顶层设计上为CRO行业提供了肥沃的土壤。
- 具体政策:
- “十四五”医药工业发展规划: 明确提出要加快创新药和高端医疗器械的研制,推动产业基础高级化、产业链现代化。
- “重大新药创制”科技重大专项: 长期以来,国家投入巨资支持新药研发,其中大量资金通过项目形式最终流向了药企和CRO,带动了整个研发链条的技术进步和能力建设。
- 税收优惠政策: 对高新技术企业、技术先进型服务企业(CRO常在此列)实行15%的优惠企业所得税率,研发费用加计扣除等政策也降低了药企的投入,间接鼓励其将研发外包。
- 对CRO的影响:
- 市场扩容: 国家战略层面的支持,使得整个医药研发市场的“蛋糕”做大,CRO作为服务提供者,自然分享到增长红利。
- 技术升级: 国家专项支持CRO在特定技术领域(如基因治疗、细胞治疗、AI药物研发等)进行攻关,提升了CRO的核心竞争力。
医保控费与支付方式改革
这类政策虽然主要是为了控制医疗费用,但客观上推动了医药产业的转型升级。
(图片来源网络,侵删)
- 具体政策:
- 国家药品集中带量采购(“集采”): 通过“以量换价”大幅降低了成熟仿制药的价格。
- DRG/DIP支付方式改革: 改变了医院按项目付费的模式,促使医院更关注成本和疗效。
- 对CRO的影响:
- 倒逼创新: “集采”使得仿制药利润空间被严重挤压,药企为了生存和发展,必须向创新药转型,这直接导致了药企对创新药研发(尤其是临床I-III期)CRO服务的需求结构性增长。
- 催生新需求: DRG/DIP等政策要求药品提供更具价值的临床证据,推动了真实世界研究的兴起,CRO的RWS业务因此成为新的增长点。
核心约束力与规范政策 (影响CRO运营与合规)
这类政策旨在规范市场秩序、保障数据质量和受试者权益,对CRO的运营提出了更高要求,提高了行业门槛。
临床试验数据核查与完整性要求
这是对CRO合规运营最严格的考验。
- 具体政策:
- 国家药监局 的飞行检查: 不定期、不打招呼地对临床试验机构和CRO进行现场检查,核查试验数据的真实性、完整性和规范性。
- 数据完整性规范: 如《药物临床试验数据现场核查要点》等,对试验数据的产生、记录、保存、报告等全过程提出了严格要求。
- 对CRO的影响:
- 合规成本上升: CRO需要投入大量资源用于内部培训、建立标准操作流程、完善质量管理体系,以应对严格的核查。
- 行业洗牌加速: 那些管理混乱、数据质量差、存在“数据造假”风险的中小型CRO将被淘汰出局,市场份额向头部、合规的CRO集中。
- 提升行业信誉: 严格的核查有助于净化行业环境,提升了中国临床数据在国际上的认可度,为CRO承接国际业务扫清障碍。
伦理审查与受试者权益保护
这是临床试验的“生命线”,也是CRO必须遵守的底线。
- 具体政策:
- 《药物临床试验质量管理规范》 的修订和强化,明确申办者、研究者、CRO在保障受试者权益方面的责任。
- 要求所有临床试验必须经过独立的伦理委员会审查批准。
- 对CRO的影响:
- 运营流程更复杂: CRO需要建立专业的伦理事务团队,确保试验方案、知情同意书等文件符合伦理要求。
- 法律风险增加: 任何涉及受试者权益的疏忽都可能导致项目叫停、罚款甚至法律诉讼,对CRO的声誉造成毁灭性打击。
数据安全与个人信息保护法规
随着数字化在CRO业务中的普及,数据安全成为新的合规重点。
(图片来源网络,侵删)
- 具体政策:
- 《中华人民共和国数据安全法》
- 《中华人民共和国个人信息保护法》
- 对CRO的影响:
- 数据管理成本增加: CRO需要对其IT系统、数据存储和传输流程进行全面的合规改造,确保临床试验中涉及的敏感患者信息得到最高级别的保护。
- 业务模式受挑战: 在数据出境、跨境数据流动等方面受到更严格的限制,对CRO开展国际多中心试验提出了新的挑战。
行业竞争与反垄断政策
随着CRO行业集中度提高,政府也开始关注其市场行为。
- 具体政策:
- 《国务院反垄断委员会关于平台经济领域的反垄断指南》 的精神同样适用于大型CRO。
- 监管机构关注是否存在“二选一”、不公平定价、滥用市场支配地位等行为。
- 对CRO的影响:
- 限制无序扩张: 防止头部CRO通过并购形成垄断,维护市场的公平竞争环境,为中小型CRO留下生存空间。
- 规范商业行为: 要求CRO在与药企的合作中保持公平、透明,避免损害客户的利益。
| 政策类别 | 具体政策 | 对CRO的直接影响 | 核心影响维度 |
|---|---|---|---|
| 驱动力 | 审评审批改革 (优先审评、MAH) | 需求爆发,业务链条延长 | 市场需求 |
| 国家创新扶持战略 | 市场扩容,技术升级 | 产业环境 | |
| 医保控费 (集采、DRG) | 倒逼创新,催生RWS新需求 | 市场结构 | |
| 约束力 | 临床试验数据核查 (飞检) | 合规成本上升,行业洗牌 | 运营合规 |
| 伦理与受试者保护 | 运营流程复杂,法律风险高 | 运营合规 | |
| 数据安全与隐私保护 | 数据管理成本增加,国际业务受限 | 运营合规 | |
| 反垄断监管 | 限制无序扩张,维护公平竞争 | 市场竞争 |
未来趋势:
影响CRO发展的政策将呈现以下趋势:
- 从“数量”到“质量”: 政策将继续鼓励创新,但更强调临床价值和真实世界证据,CRO需要提供更高质量、更具深度的数据分析和解决方案。
- 从“单一”到“综合”: 药企对CRO的需求不再局限于临床试验,而是希望CRO能提供从早期发现、临床开发到商业化生产的一站式、端到端服务,一体化、平台化的CRO将更具优势。
- 从“中国”到“全球”: 随着中国CRO能力的提升和成本的竞争力,政策将鼓励其“走出去”,承接更多国际多中心试验和
文章版权及转载声明
作者:99ANYc3cd6本文地址:https://bj-citytv.com/post/37.html发布于 2025-11-28
文章转载或复制请以超链接形式并注明出处北京城市TV