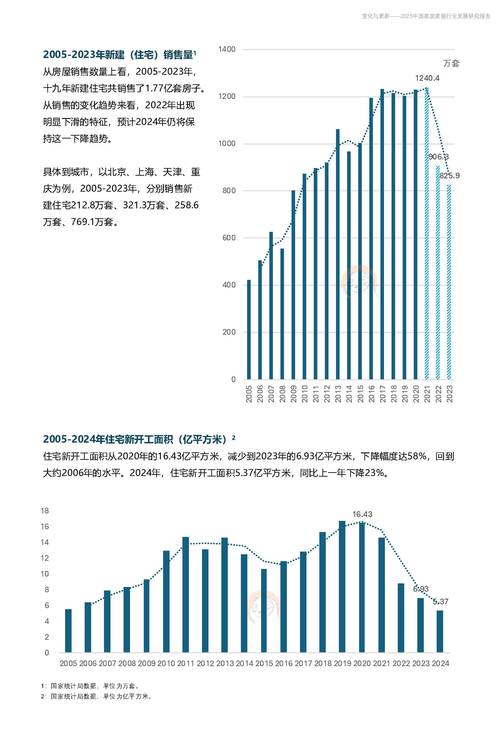
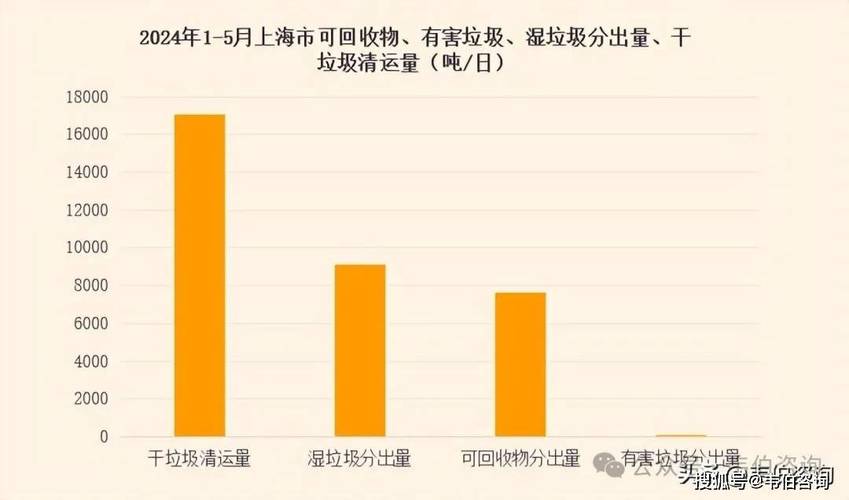
催化剂真的不影响反应趋势吗?
这个说法是完全正确的,这是一个化学中的基本且非常重要的概念。
(图片来源网络,侵删)
我们可以从热力学的角度来理解这一点,一个化学反应能否发生,以及进行的趋势有多大,是由热力学决定的,而催化剂的作用属于动力学范畴。
下面我们来详细解释:
什么是“反应的趋势”?
“反应的趋势”在化学中通常指以下两点:
- 反应的自发性:一个反应在给定条件下是否能自发进行,这由吉布斯自由能变 (ΔG) 决定。
- ΔG < 0,反应在热力学上是自发的,可以正向进行。
- ΔG > 0,反应在热力学上是非自发的,不能正向进行(但其逆反应是自发的)。
- 反应的限度:一个自发反应能进行到什么程度,达到平衡时各物质的浓度是多少,这由化学平衡常数 (K) 决定。
K 值越大,意味着反应越完全,产物越多。
(图片来源网络,侵删)
核心点:ΔG 和 K 都是由反应物和产物的自身性质(如键能、熵等)以及反应条件(如温度、压力)决定的,它们与反应的路径无关。
催化剂的作用是什么?
催化剂是一种能改变反应速率,但在反应前后质量和化学性质不变的物质。
- 如何改变速率? 催化剂通过提供一个全新的、活化能更低的反应路径,来同时降低正反应和逆反应的活化能 (Ea)。
- 想象一座山,反应物和产物分别位于山的两侧,山的高度就是活化能,自发反应是从高处(反应物)流向低处(产物)。
- 没有催化剂时,你必须翻过整座高山(高活化能),过程很慢。
- 加入催化剂,相当于在山中挖了一条隧道,你仍然是从高处到低处,但走隧道(低活化能)的速度快得多。
- 关键特征:
- 只改变速率,不改变平衡:因为催化剂同等程度地降低了正反应和逆反应的活化能,所以它缩短了达到平衡的时间,但不会改变平衡点的位置,这意味着,达到平衡后,反应物和产物的浓度比例(由K决定)和没有催化剂时是一样的。
- 不改变ΔG:因为反应的始态(反应物)和终态(产物)没有改变,所以反应的吉布斯自由能变 (ΔG) 也不变,催化剂不能让一个在热力学上不能发生的反应(ΔG > 0)自发进行。
一个生动的比喻
- 热力学(反应趋势):决定了水会不会从高处流向低处,只要高处有水,它就有流向低处的趋势,这个趋势是客观存在的,由水位差(势能差)决定。
- 动力学(反应速率):决定了水流的速度,你可以挖一条很宽的河道(催化剂),让水流得飞快;也可以用石头堵住河道,让水流变得非常慢甚至停止(抑制剂),但无论你怎么改变水流速度,只要河道两端的水位差不变,水流的最终趋势(从高到低)是不会改变的。
| 特性 | 热力学 (反应趋势) | 动力学 (反应速率) |
|---|---|---|
| 决定因素 | 反应物和产物的性质、温度、压力 | 催化剂、温度、浓度、反应物接触面积等 |
| 核心参数 | 吉布斯自由能变 (ΔG)、平衡常数 (K) | 活化能 (Ea)、反应速率 |
| 催化剂的影响 | 无影响 | 有显著影响:降低活化能,加快反应速率 |
| 通俗比喻 | 水是否会从高处流向低处 | 水流得快还是慢 |
催化剂就像一个高效的“交通协管员”,它指挥着反应物分子更快地找到通往产物的“捷径”,但它不能改变反应的“目的地”(产物)和“出发点”(反应物)之间的能量高低关系(ΔG),催化剂不影响反应的趋势,只影响反应达到平衡的速度。
文章版权及转载声明
作者:99ANYc3cd6本文地址:https://bj-citytv.com/post/5319.html发布于 01-26
文章转载或复制请以超链接形式并注明出处北京城市TV