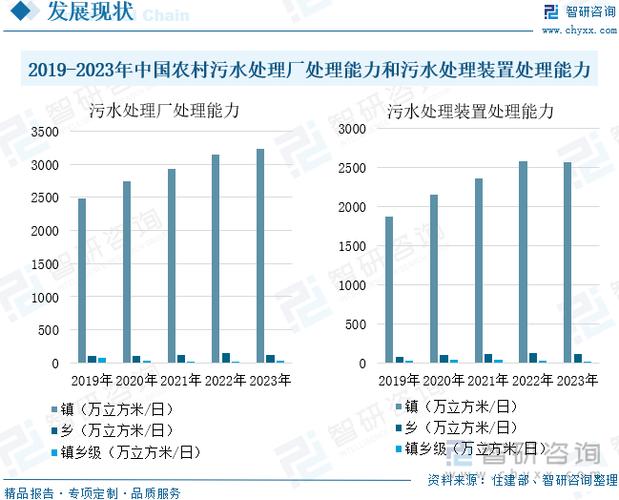
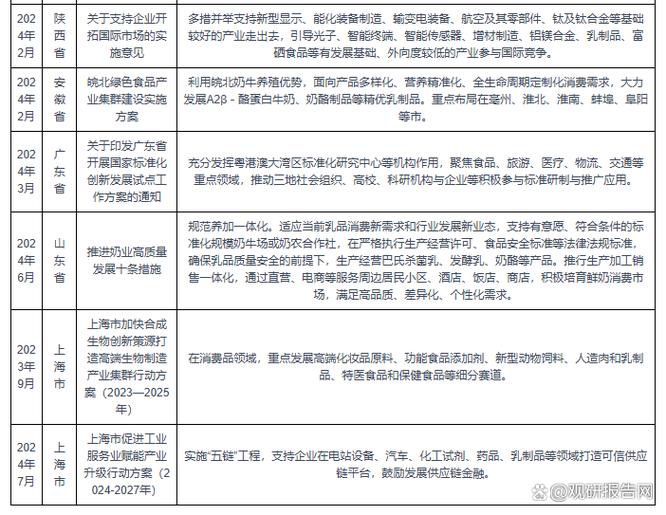
国外生物医药产业政策
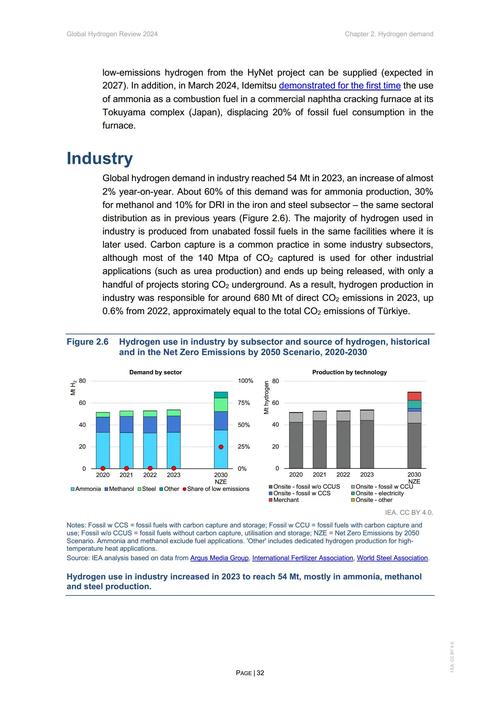
生物医药产业是全球竞争的战略性新兴产业,具有高投入、高风险、高回报、长周期的特点,世界各国政府都将其视为国家竞争力的核心组成部分,通过制定和实施一系列复杂的政策组合拳,来引导和扶持其发展。
(图片来源网络,侵删)
以下将从政策目标、核心政策工具、主要国家/地区模式和未来趋势四个维度,为您详细解读国外的生物医药产业政策。
政策核心目标
各国的生物医药产业政策虽然具体措施各异,但核心目标高度一致,主要包括:
- 提升国民健康水平:通过鼓励创新药物和疗法的研发,解决未被满足的临床需求,攻克癌症、阿尔茨海默病、罕见病等重大疾病。
- 增强国家经济竞争力:打造世界领先的生物医药产业集群,吸引全球资本和人才,创造高技能就业岗位,并形成出口优势。
- 保障药品可及性与可负担性:在激励创新的同时,确保患者能够获得并负担得起所需的药品,这是一个永恒的平衡难题。
- 维护公共卫生安全:建立强大的疫苗、抗病毒药物和诊断工具研发生产能力,以应对全球性大流行病等突发公共卫生事件。
核心政策工具
为实现上述目标,各国政府主要运用以下几类政策工具:
研发激励政策
这是最核心、最直接的支持手段,旨在降低研发风险和成本。
(图片来源网络,侵删)
- 研发税收抵免:允许企业将研发投入的一定比例(如美国的20%-30%)从应纳税所得额中扣除,直接减轻税负,美国《通胀削减法案》进一步加强了这一政策。
- 政府直接资助:
- 基础研究:通过国家级科研机构(如美国国立卫生研究院NIH、英国医学研究理事会MRC)提供大量竞争性科研经费,支持大学和科研院所的基础生物学和医学研究。
- 转化研究:设立专项基金(如美国国立卫生研究院的转化医学中心、欧盟的“地平线欧洲”计划),资助从实验室到临床的转化研究。
- 专利保护:通过授予药品专利(通常为20年),确保研发企业在专利期内拥有市场独占权,从而收回高昂的研发成本并获取利润,这是激励创新的根本制度保障。
- 孤儿药资格认定:为罕见病药物提供额外激励,如7年的市场独占期(在美国),并减免新药申请费用,鼓励企业开发针对患者人数少的疾病的药物。
审评审批与市场准入政策
旨在加速创新疗法上市,同时确保其安全有效。
- 加速审评通道:
- 突破性疗法认定:针对治疗严重疾病的药物,如果初步临床数据显示其可能显著优于现有疗法,可享受滚动审评、密集沟通等优先审评服务。
- 快速通道:用于治疗严重或危及生命的疾病,允许在研发期间与FDA更早、更频繁地互动,并提交部分申请批次。
- 优先审评:将审评时间从标准的10个月缩短到6个月。
- 有条件批准/附条件上市许可:针对治疗严重疾病的药物,在确证性临床完成前,可根据替代终点或临床获益等早期证据批准上市,要求企业上市后继续完成确证性研究。
- 实审评:FDA等机构在审批期间不要求提交新的动物或人体研究数据,而是基于已有数据进行科学评估,大幅缩短了审批时间。
- 适应症外推:基于一项临床试验的结果,可以推断该疗法在其他相关患者群体中也同样有效,从而扩大了患者覆盖面,提高了研发效率。
医疗支付与定价政策
这是连接创新与市场的关键,直接影响企业的收入和患者的可及性。
- 创新支付模式:
- 基于价值的定价:药品价格与其临床价值(如延长生命、提高生活质量)挂钩,英国NICE的“质量调整生命年”是典型代表。
- 分期付款/风险分担协议:如果药品在真实世界中的疗效未达到预期,企业可部分或全部退还费用,德国、法国等正在探索此类模式。
- 按疗效付费:只有在患者取得特定疗效时,医保才支付费用。
- 医保覆盖与准入谈判:
- 强制/自愿医保准入谈判:许多国家(如德国、法国、日本、加拿大)拥有强大的国家或区域医保体系,会与制药企业进行价格谈判,以将创新药纳入医保报销目录,美国的《通胀削减法案》首次授权联邦医保对部分高价药品进行价格谈判,这是一个重大转折。
- 外部参考定价:将本国药品价格与参考国家(如德国、法国、英国、意大利)的价格进行比较,以此作为定价的基准。
产业生态与资本政策
旨在构建完整的产业链和良好的创新环境。
- 产业集群建设:政府通过规划园区、提供基础设施和优惠政策,吸引上下游企业、研究机构和资本聚集,形成“产学研医”紧密结合的创新生态系统,美国波士顿、旧金山,英国剑桥,瑞士巴塞尔等都是全球著名的生物医药集群。
- 鼓励风险投资:通过税收优惠、政府引导基金等方式,鼓励私人资本投向早期生物医药初创公司,解决其“死亡谷”阶段的融资难题。
- 人才培养与引进:改革移民政策,吸引全球顶尖科学家和企业家;加强本国STEM(科学、技术、工程、数学)教育,培养后备人才。
主要国家/地区模式比较
| 国家/地区 | 核心特点与政策亮点 | 优势 | 挑战 |
|---|---|---|---|
| 美国 | 市场驱动,创新活力最强 强大的研发投入:NIH是全球最大的生物医学研究资助者。 灵活的审评体系:FDA拥有最完善的加速审评工具箱,引领全球审评标准。 资本市场成熟:风险投资和IPO渠道畅通,为初创企业提供充足“弹药”。 《通胀削减法案》:首次赋予联邦医保对部分药品的定价谈判权,试图平衡创新与可及性。 |
创新源头:拥有全球最多的创新药企和专利技术,新药首发上市率最高。 | 医疗成本高企:药品价格昂贵,医疗体系不平等问题突出,政府与药企在定价上的矛盾日益尖锐。 |
| 欧盟 | 福利导向,注重公平与可及性 分散化与集中化结合:各成员国(如德国、法国)有独立的定价和医保准入体系,同时EMA提供统一的药品上市许可。 严格的成本效益评估:以NICE为代表的机构,通过QALY等工具进行严格的“价值评估”,是药品能否进入市场的关键门槛。 鼓励罕见病和抗生素研发:有完善的孤儿药和抗生素奖励计划。 |
药品可及性高:通过强力的价格谈判,使得欧盟国家药品价格普遍低于美国。 | 创新激励相对不足:过于严格的成本控制可能削弱企业研发高价值创新药的意愿,新药首发上市率低于美国。 |
| 日本 | “先创新,后仿制”的追赶模式 加速审评与市场独占期:对全球首创新药给予较长的审评时间和市场独占期,以吸引外资药企将日本作为首发市场之一。 积极的医保覆盖:只要药品被承认有效,通常能快速进入医保报销,患者自付比例低。 政府主导的产业培育:通过“生命创新区”等项目,大力扶持本土生物技术公司。 |
市场准入快:是全球第二大医药市场,对新药的需求和支付能力都很强。 | 研发能力仍待提升:本土企业虽强,但在全球领先的原创性突破方面与美国仍有差距。 |
| 英国 | 国家主导的“价值购买者”典范 NICE的核心地位:其评估结果直接决定药品能否被NHS(国家医疗服务体系)报销,对全球药品定价有巨大影响力。 强制性的价格管制:PAGB(药品价格管制方案)对非专利药和部分专利药进行严格的价格控制。 强大的科研基础:拥有牛津、剑桥等世界顶尖的生物医学研究机构。 |
医疗体系效率与公平性:NICE模式试图在有限的预算内实现医疗资源的最大化利用。 | 创新与预算的永恒矛盾:NICE的苛刻标准经常导致一些突破性疗法因“性价比不高”而被拒之门外,引发社会争议。 |
未来趋势与挑战
全球生物医药产业政策正面临新的变革,主要趋势包括:
(图片来源网络,侵删)
- 从“鼓励创新”到“平衡创新与可及性”:随着医疗支出压力增大和公众对药价的关注,各国政府都在探索新的定价和支付模式,试图在保护创新激励的同时,更好地控制成本,美国的药品价格谈判是这一趋势的最显著标志。
- 拥抱颠覆性技术:针对细胞与基因治疗、mRNA、AI药物发现等前沿技术,各国正在制定专门的监管框架和支付政策,以适应其“一次治疗、长期治愈”或高度个性化的特点。
- 强化供应链安全与韧性:新冠疫情暴露了全球医药供应链的脆弱性,各国政策正从单纯的成本效率导向,转向兼顾安全、多元和本土化的供应链战略。
- 数据驱动的决策:利用真实世界数据和人工智能来辅助药品审评、价值评估和价格谈判,将成为未来的重要方向。
- 国际合作与竞争并存:在研发标准、数据共享、应对全球疫情等方面需要国际合作,但在技术、人才和市场准入方面的竞争也日趋激烈。
国外生物医药产业政策是一个复杂而精密的系统,它通过研发激励、审评加速、支付改革和生态建设四大支柱,动态地平衡着创新、成本、公平和安全这四个核心目标,不同国家根据其历史、文化和经济体制,选择了不同的政策组合:美国以市场活力见长,欧盟以福利公平为重,日本和英国则在追赶与管控之间寻找平衡。
随着技术的飞速发展和全球性挑战的增多,各国的生物医药政策将继续演变,其核心将是如何在一个更加复杂的环境中,更好地守护人类健康并驱动经济前行,对于中国等新兴市场而言,深入研究并借鉴这些国际经验,对于制定出适合自身国情的生物医药发展战略至关重要。
文章版权及转载声明
作者:99ANYc3cd6本文地址:https://bj-citytv.com/post/3336.html发布于 01-06
文章转载或复制请以超链接形式并注明出处北京城市TV